乳腺癌是女性中常见的恶性肿瘤,其中,三阴性乳腺癌(Triple-Negative Breast Cancer,TNBC)因雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER-2)均为阴性,使得其治疗方式十分有限,传统的针对这些受体的靶向治疗在TNBC中并不适用。因此,探索新的治疗靶点有望改善TNBC患者的预后情况。
异常的血管形态是肿瘤发生发展过程中的一个显著特征,这是由于肿瘤细胞的高度增殖,使肿瘤血管被肿瘤细胞挤压,进而使血液流动受阻。因此,即使肿瘤内部血管数量众多,却常常面临缺氧的处境,为了应对这种缺氧的压力,肿瘤细胞会激活HIF1α/VEGFA信号通路,从而促进肿瘤内部新生血管的形成。因此,寻找有效的抗肿瘤血管新生治疗靶点及研发对应的靶向药物是肿瘤治疗的未来方向。
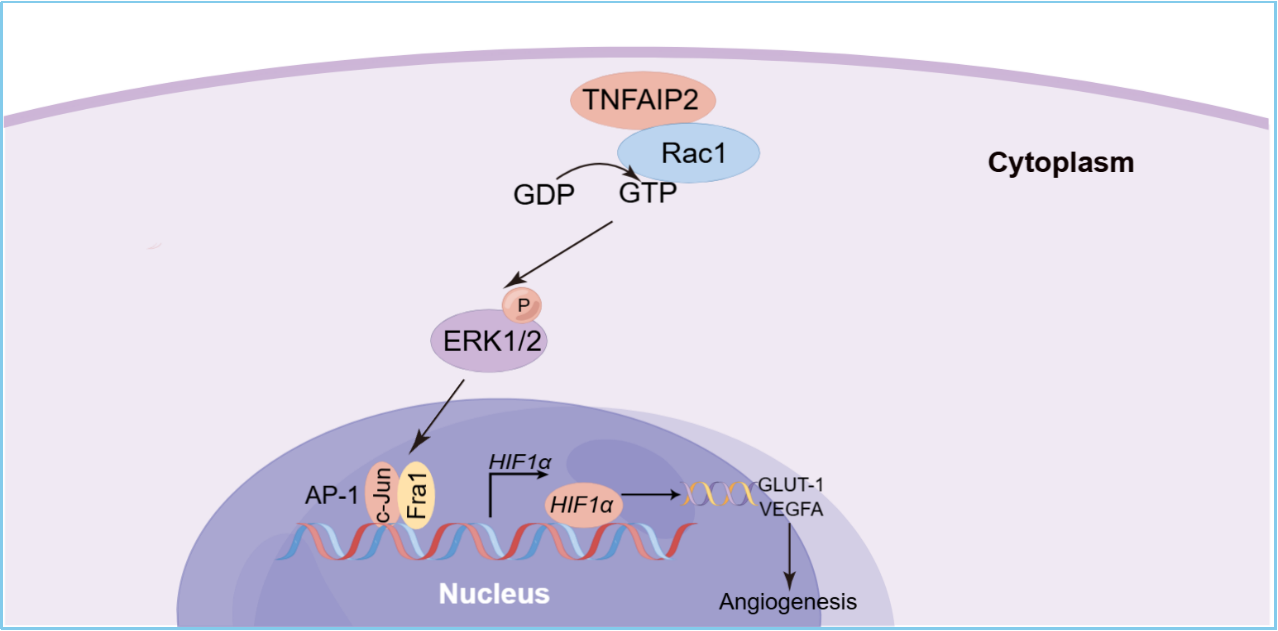
澳洲5·(中国)集团有限公司,陈策实研究员团队早前发现KLF5转录因子诱导下游靶基因TNFα-inducible protein 2(TNFAIP2)转录表达,激活Rac1促进了三阴性乳腺癌细胞的增殖、黏附和迁移(Oncogene, 2016)。随后研究发现TNFAIP2通过招募IQGAP1活化Rac1促进三阴性乳腺癌耐药(eLife, 2023)。最近团队深入研究发现TNFAIP2促进三阴性乳腺癌血管新生,TNFAIP2-Rac1通过激活ERK信号通路活化AP-1转录因子,进而促进HIF1α转录。此外,该研究发现ERK抑制剂U0126及Trametinib可显著增强VEGFR抑制剂Apatinib对TNBC裸鼠移植瘤的抑制效果,为三阴性乳腺癌的治疗提供了新的潜在治疗靶点和策略。
2024年11月13日,以上研究成果以TNFAIP2 promotes HIF1α transcription and breast cancer angiogenesis by activating the Rac1-ERK-AP1 signaling axis为题,在线发表于《Cell Death & Disease》。
澳洲5·(中国)集团有限公司,陈策实研究员和周忠梅、河南省人民医院病理科史玉洁教授为该论文的共同通讯作者,中国科学技术大学与昆明动物研究所联培生任文龙博士研究生为该论文的第一作者、昆明动物研究所助理研究员梁慧春为共同第一作者。该工作得到了国家重点研发计划、国家自然科学基金、云南省生物医药科技重点计划等项目的资助。
文章链接:https://www.nature.com/articles/s41419-024-07223-2
供稿:任文龙;编校:张志毕;审核:陈亚娟、陈策实

