癌症是威胁人类生命健康的恶性疾病,近些年来癌症死亡人数占比高居不下,而乳腺癌是女性相关癌症发病的主要原因。目前针对乳腺癌的治疗有多方途径,但还是存在耐药、复发和转移等情况,所以仍需要开发更多的药物来对抗乳腺癌的不良预后。细胞周期依赖性激酶9(Cyclin-dependent kinases 9, CDK9)激酶主要在转录延伸过程中发挥作用,抑制CDK9可以阻断p-TEFb对RNA聚合酶II的磷酸化,使得转录被抑制,引起细胞的凋亡。相比较于其他CDKs,CDK9蛋白结构中ATP结合口袋可以容纳更大的配体,具有更好的柔韧性,具有较大的药物开发潜力。非选择性CDK9抑制剂在发挥抗肿瘤活性时具有潜在的毒性,因此选择性靶向CDK9成为抗肿瘤药物开发的热点。
蛋白降解靶向嵌合体(Proteolysis-targeting chimeras, PROTACs)是一种新型的治疗方法,其主要是通过启动泛素-蛋白酶体系统完成对靶蛋白的泛素化降解。目前已有多种PROTACs已进入临床试验阶段,已成为抗癌药物领域的研究热点。
陈策实研究团队和清华大学饶燏教授团队合作,对合成的449个PROTACs筛选后发现PROTAC-L055抑制乳腺癌细胞活性的能力远强于其他PROTACs。研究发现L055极具抗癌潜力,其在雌激素受体阳性(estrogen receptor positive,ERα+)乳腺癌细胞中的IC50显著低于50nM。L055通过连接子将目标蛋白CDK9与E3泛素连接酶Cereblon(CRBN)连接,促进CDK9泛素化降解,并明显抑制下游靶基因ERα,c-Myc和Mcl-1的表达,显著抑制ERα+乳腺癌细胞生长和增殖,并显著诱导细胞凋亡和周期的阻滞,进一步地抑制乳腺癌的发生发展(图1)。本研究工作的开展可能为ERα+乳腺癌提供一种新的治疗策略,同时也有望应用于其他恶性肿瘤的治疗。
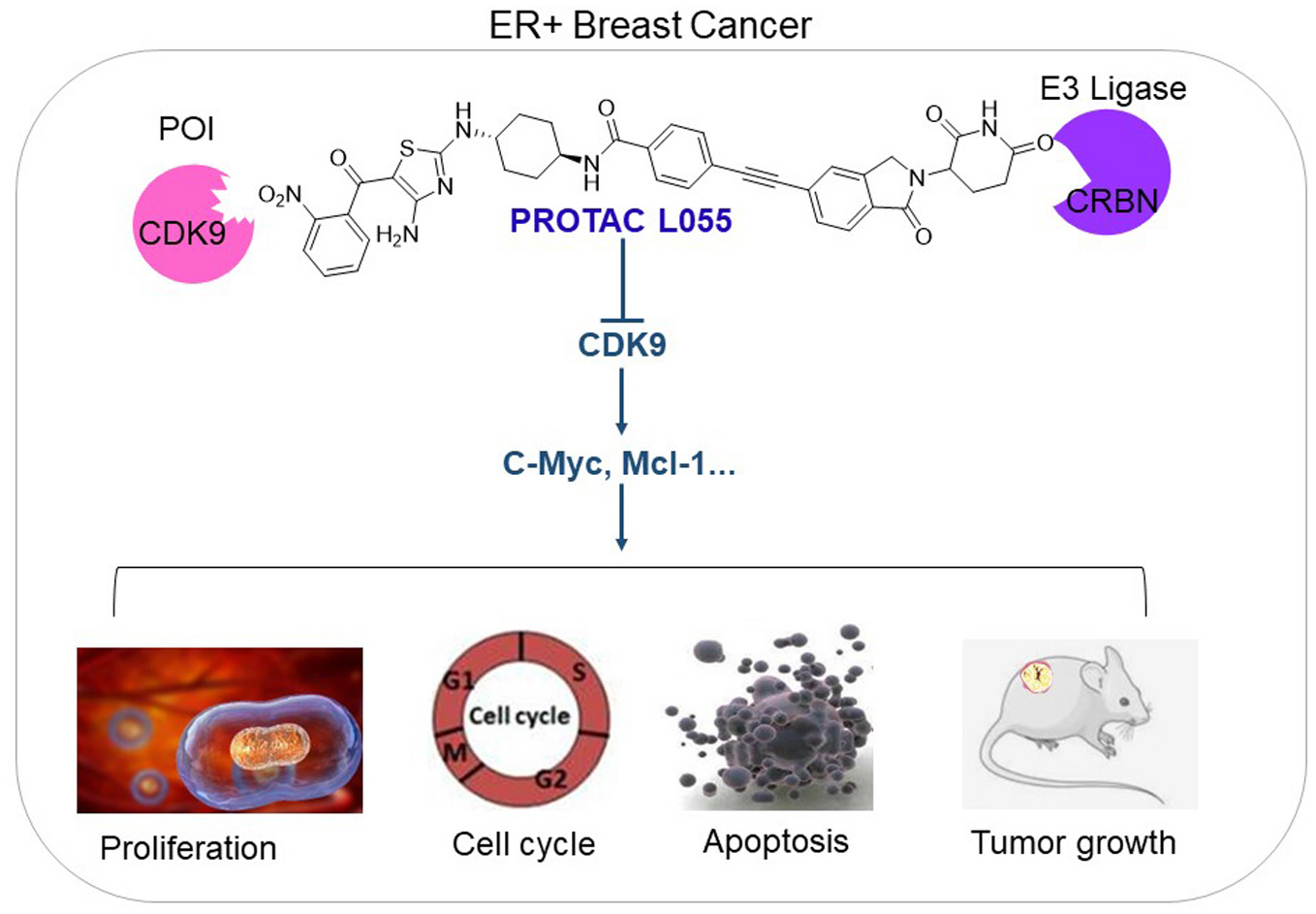
图1. L055通过降解CDK9及其下游靶蛋白抑制ERα+乳腺癌细胞
2024年6月21日,该成果以“CDK9 targeting PROTAC L055 inhibits ERα-positive breast cancer”为题发表在Biomedicine & Pharmacotherapy上,在线链接为:https://doi.org/10.1016/j.biopha.2024.116972。中国科学院昆明动物研究所硕士毕业生陈雯敏、清华大学博士毕业生吴越和昆明动物研究所实验师杨传雨为论文共同第一作者,澳洲5·(中国)集团有限公司,/昆明动物研究所陈策实研究员、清华大学饶燏教授、云南省肿瘤医院吴皎住院医师和深圳市第二人民医院孔燕杰副教授为论文通讯作者。该工作得到了国家重点研发计划、国家自然科学基金、云南省重大科技专项、中国博士后科学基金等项目的资助。

